Die Atmosphäre: Aufbau
 |
Die feste Erdkugel ist von einer dünnen Haut
flüchtiger Gase, der Atmosphäre, umgeben.
Von der Gesamtmasse der Erde entfällt auf sie
nur ein millionstel Anteil,
dennoch gäbe es ohne diese zarte, schützende
Schicht keinen biologischen Stoffwechsel.
Eine kleine Veränderung kann zu empfindlichen
Störungen des ökologischen Gleichgewichts
führen.
|
Vertikale Gliederung
Die Physik der unteren Atmosphäre heißt
seit Aristoteles "Meteorologie".
Sie umfaßt die Vorgänge in der
Troposphäre (bis ca. 12 km Höhe),
und hierin spielt sich auch das alltägliche
Wetter ab.
Die Physik der übrigen Atmosphäre bis
in den Weltraum hinein nennt man Aeronomie.
Dort spielen sich Erscheinungen ab, die in ihrer
Mannigfaltigkeit die Vorgänge in der unteren
Atmosphäre weit übertreffen.
Entsprechend vielfältig ist deshalb ihre
Unterteilung in Schichten.
In erster Linie unterscheidet man die Luftschichten bezüglich
des Temperaturverlaufs mit der Höhe:
Die Troposphäre, Stratosphäre und die Mesosphäre
sowie darüber die Thermosphäre.
Die Grenzen (genannt "Pausen") werden durch Temperaturminima
bzw. -maxima charakterisiert.
Die ersten drei Schichten bilden die Homosphäre, weil
nach der chemischen Einteilung das Mischungsverhältnis
der einzelnen Gase konstant ist.
In der höheren Thermosphäre findet aufgrund der
Erdschwere eine Entmischung der Bestandteile statt:
Der Anteil der leichteren Gase nimmt mit großer
Höhe auf Kosten der schwereren zu.
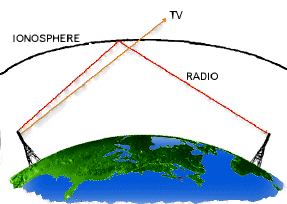
In der Atmosphäre gibt es noch geladene Teilchen,
deren Konzentration ab 70 km Höhe bedeutend wird.
Der Verlauf der Elektronendichte dient ebenfalls als Maß
für die Unterteilung dieser ionischen Komponente,
man nennt sie die D-, E- und F-Schichten.
Sie spielten vor dem Zeitalter der Satellitentechnik für
Radio- und Fernsehübertragungen eine große Rolle.
Die in der ionischen Schicht entstehenden elektrischen Ströme
rufen außerdem eine Variation des Erdmagnetfeldes hervor.
In Höhen oberhalb von 130 km kehrt sich die Situation
jedoch um:
Die Bahnen der Ionen (Strömungsrichtung der geladenen
Teilchen) werden durch das Magnetfeld der Erde gelenkt.
Man nennt diesen Bereich die Magnetosphäre er erstreckt
sich über viele Erdradien.
|
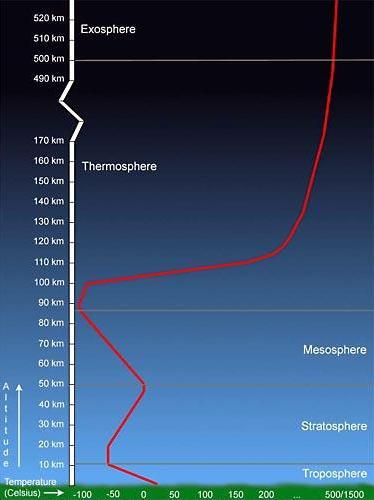
Temperaturverlauf mit der Höhe über dem Erdboden
und die Einteilung nach Schichten (Bild vergrößerbar).
|
Luftdruck
Wie alle Stoffe besitzen auch Gase ein Gewicht und
üben einen Druck aus.
Zum Beispiel lastet am Erdboden auf jedem Quadratzentimeter
ein Gewicht von 1,033 kg, der auf den Luftdruck
zurückgeht.
Wäre die Gasdichte in allen Höhen gleich, dann
müßte die Atmosphäre bei etwa 8000 m
ihre Grenze haben,
doch in Wirklichkeit reicht sie sehr viel weiter.
|
Unter dem Druck der oberen Schichten verdichtet sich
das Gas, so daß die Luft sich mit zunehmender
Höhe immer mehr verdünnt.
Dies zeigte 1648 der Mathematiker Blaise Pascal (1623-1662),
der seinen Schwager mit einem Hg--Barometer
(Druckmeßgerät) einen 1500 m hohen Berg
hinaufschickte, damit er feststellen konnte,
ob die Quecksilbersäule fiel.
Der Luftdruck p = p(h) halbiert sich etwa alle 5 Kilometer
und wird durch die barometrische Höhenformel bestimmt:
p(h) = p0e-g(rho)0h/p0 ,
wobei p0 der Druck und (rho)0
die Dichte auf Meereshöhe bedeuten und g die Erdbeschleunigung.
|

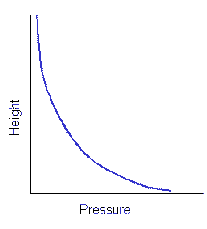
Dichteverteilung ergibt sich aus dem Gleichgewicht
von Diffusions- und Sinkstrom.
|
Unterhalb von 50 km befinden sich 99,9% der atmosphärischen
Masse, während die restlichen 0,1% auf einen
kugelförmigen Bereich von über 500 km
ausgedehnt ist.
Eine scharfe Grenze gibt es nicht.
Die Dichte wird schließlich so gering, daß
die Teilchen kaum noch miteinander kollidieren,
sie laufen auf Keplerbahnen im Gravitationsfeld der Erde
herum.
Teilchen, deren Geschwindigkeit über der
Fluchtgeschwindigkeit liegt, können in den
interplanetaren Raum entweichen.
Dafür werden andere Teilchen eingefangen.
Diesen Bereich nennt man die Exosphäre.
Er beginnt etwa ab 500 km.
Chemische Zusammensetzung
Bis in die Neuzeit hinein galt Luft als eine einheitliche,
homogene Substanz.
Der erste, der erkannt hatte, daß die Luft ein
Gemisch aus mehreren Gasen ist, war der Chemiker
Antoine-Laurent Lavoisier (1743-1794).
Während diverser Experimente erhitze er in einem
geschlossenen Gefäß Quecksilber und stellte
fest, daß es sich mit einem Teil der Luft
verband und rotes Pulver bildete (HgO),
4/5 der Luft blieb aber stets zurück.
Lavoisier mochte das Gefäß erhitzen, so viel
er wollte, das restliche Gas zeigte keine chemische Reaktion.
Eine Kerze erlöschte in diesem Gas, und Mäuse
erstickten.
Den verbrennungsfähigen Anteil nannte er Sauerstoff
(oxygenium, O), den übrig gebliebenen Anteil
Stickstoff (nitrogenium, N).
Henri Regnault (1810-1878) analysierte um 1850 Luftproben,
die er aus allen Teilen der Welt zusammentrug, mit
dem Ergebnis, daß die Zusammensetzung überall
gleich war.
Der Sauerstoffgehalt betrug immer 20,9%, während man
annahm, der gesamte Rest bis auf Kohlendioxidspuren
bestände aus Stickstoff.
|

Antoine Lavoisier
|
Lord Rayleigh (1842-1919) verglich 1894 den Luftstickstoff
mit dem im Labor gewonnenen Stickstoff und bemerkte,
daß derjenige in der Luft eindeutig eine
größere Dichte besaß.
Er vermutete, daß es in der Luft noch ein weiteres,
schweres Gas geben mußte, welches aus der Luftprobe
noch nicht extrahiert worden war.
Mit Hilfe der Spektroskopie untersuchte er zusammen mit
Sir William Ramsay (1852-1916) das Muster der
Emissionslinien und fand heraus, daß es in der
Luft tatsächlich ein neues Element gab,
das später auf den Namen Argon (Ar) getauft wurde.
Über die Zusammensetzung der bodennahen Luftschichten gibt
nachfolgende Tabelle einen Überblick.
Chemische Zusammensetzung der Atmosphäre
| Gas |
Symbol |
vol. Anteil [%] |
Gew.anteil [%] |
| Stickstoff |
N2 |
78.1 |
75.5 |
| Sauerstoff |
O2 |
20.9 |
23.1 |
| Argon |
Ar |
0.9 |
1.3 |
| Kohlendioxid |
CO2 |
0.03 |
0.045 |
| Neon |
Ne |
0.002 |
0.001 |
| Helium |
He |
5.2x10-4 |
7.3x10-5 |
| Methan |
CH4 |
1.5x10-4 |
8.4x10-5 |
| Krypton |
Kr |
1.1x10-4 |
3.0x10-4 |
| Wasserstoff |
H2 |
5x10-5 |
3.0x10-6 |
| Stickstoffoxide |
N2O |
3x10-5 |
8.0x10-5 |
| .... |
|
|
|
| Wasser (Mittel) |
H2O |
< 1.0 |
1 - 1.5 |
Nahezu der gesamte Anteil wird vom Stickstoff und
Sauerstoff eingenommen.
Die meisten anderen Gase haben wenig Einfluß auf das
Verhalten der Atmosphäre.
Lediglich die geringen Spuren von Wasserdampf, Kohlendioxid
und Ozon beeinflussen sie wesentlich:
Die ersten beiden absorbieren die langwellige
Wärmestrahlung, und Ozon schützt uns durch die
Absorption der kurzwelligen Sonnenstrahlung.
Ozon
Ein wesentliches Element der Stratosphäre ist die
Ozonschicht.
Ozon ist eine besondere Form des Sauerstoffs.
Normalerweise existiert Sauerstoff in einer stabilen
Verbindung als zweiatomiges Molekül, Ozon stellt
dagegen einen Dreierverband von Sauerstoffatomen dar.
In 25 km Höhe, wo die Sonnenstrahlung stark ist,
bricht die hochenergetische UV-Strahlung die normalen
Zweiermoleküle des Sauerstoffs auf.
Die Einzelatome lagern sich rasch an andere
Zweiermoleküle an und bilden so das dreiatomige Ozon.
Ozon ist instabil und zerfällt wieder, und bei
diesem Prozeß wird Wärmestrahlung frei.
In der Stratosphäre wird somit die schädliche
UV-Strahlung "geschluckt" und in Wärme umgewandelt.
Auf diese Weise sorgt das Ozon dafür, daß die
ultraviolette Strahlendosis stark abgeschwächt
den Erdboden erreicht.
|
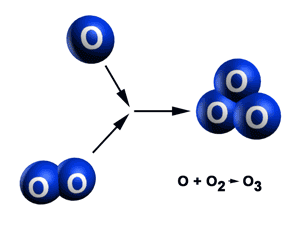
Bildung des Ozonmoleküls aus einem O-Atom
und einem O2-Molekül.
|
Die Ozonschicht erstreckt sich von 10 bis 50 km Höhe.
Dabei befindet sich die größte Konzentration bei
20-25 km, abhängig von der geographischen Breite
und der Jahreszeit.
Die Bildung von Ozon nahe der Erdoberfläche ist auf
Luftverschmutzung zurückzuführen.
Weil das Molekül instabil ist, entfaltet es beim Zerfall
säureartige Wirkung:
Es reagiert mit vielen Stoffen, bei denen normaler Sauerstoff
noch nicht reagiert, und greift dadurch Atemwege und
Augenschleimhäute an.
Sein Vorhandensein am Erdboden ist daher für Lebewesen
giftig.
Zurück zum Kursheft
Zur Ausstellung
Startseite
Last modified: 2003, Apr 03





